Une réaction acido-basique met en jeu deux couples acide-base : le couple Acide 1 / Base 1 et le couple Acide 2 / Base 2 . Une réaction acide-base est une transformation chimique entre l'acide d'un couple et la base d'un autre couple acide/base, par l'intermédiaire d'un échange d'ions H + . Pour équilibrer l'équation de la réaction qui a.. On raisonnera comme pour l'acide totalement dissocié dans l'eau, on considèrera que la base dosée est OH-(aq) et on utilisera une solution d'acide chlorhydrique pour effectuer ce dosage. d. 4ème cas : on veut titrer une base dont la dissociation est limitée dans l'eau :

Couples acide base YouTube

La force des acides et des bases en solution aqueuse Tle Cours PhysiqueChimie Kartable

Comment identifier les couples acide/base ? Méthode Terminale spécialité Chimie YouTube

Acidebase (couple et demiéquation) Terminale Chimie YouTube

Les réactions acide base YouTube

1Formation Théorie acidobasique
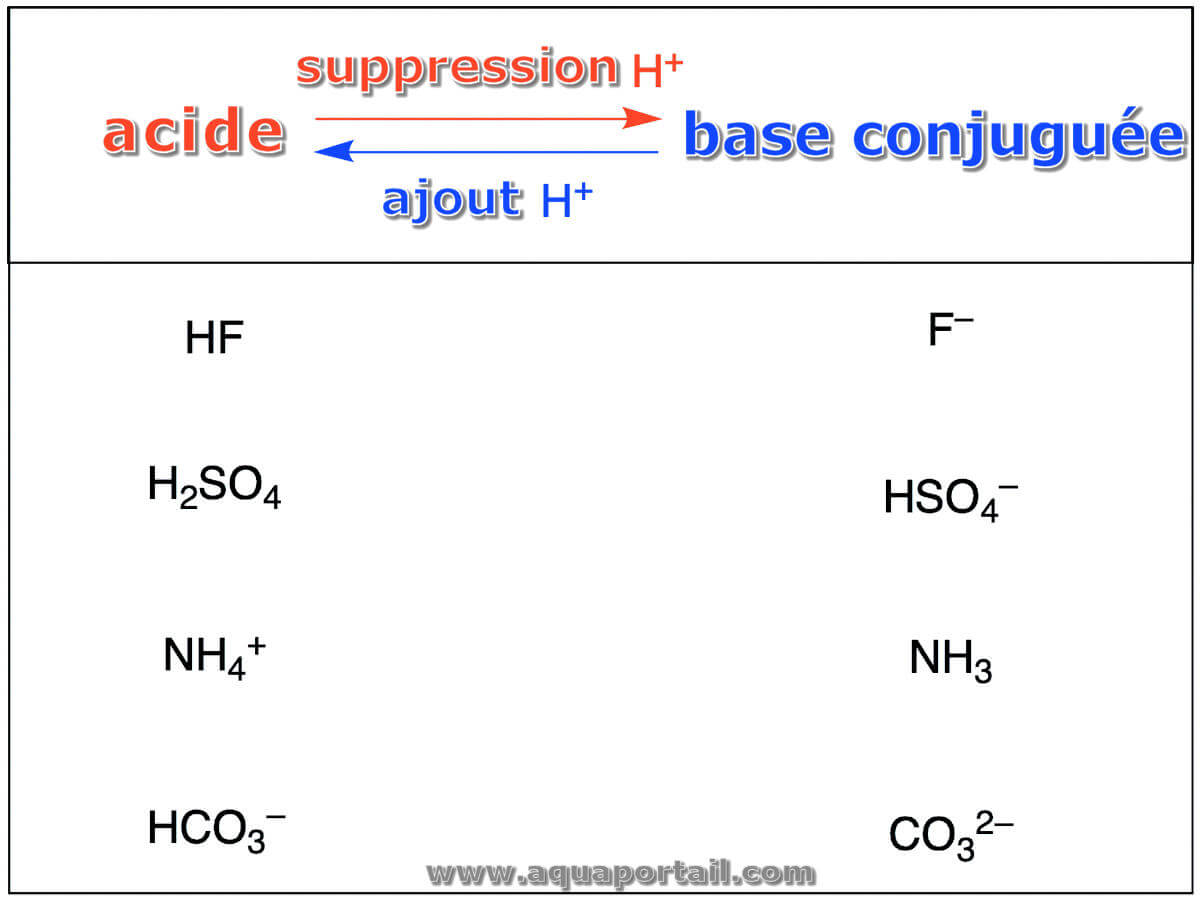
Base conjuguée définition et explications
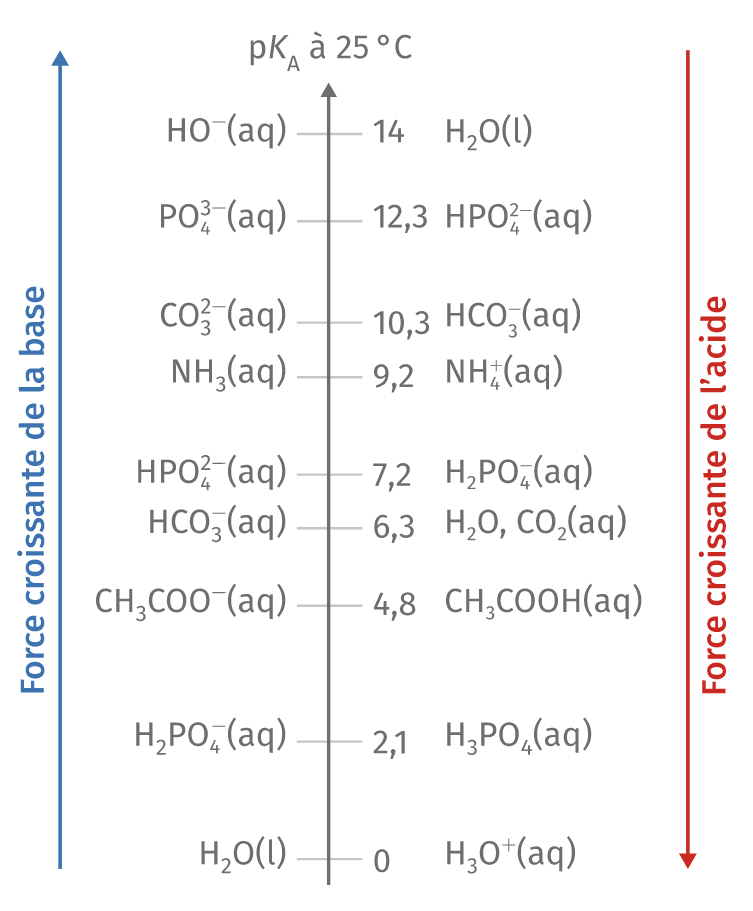
Force des acides et des bases Evolution spontanée d’un système chimique
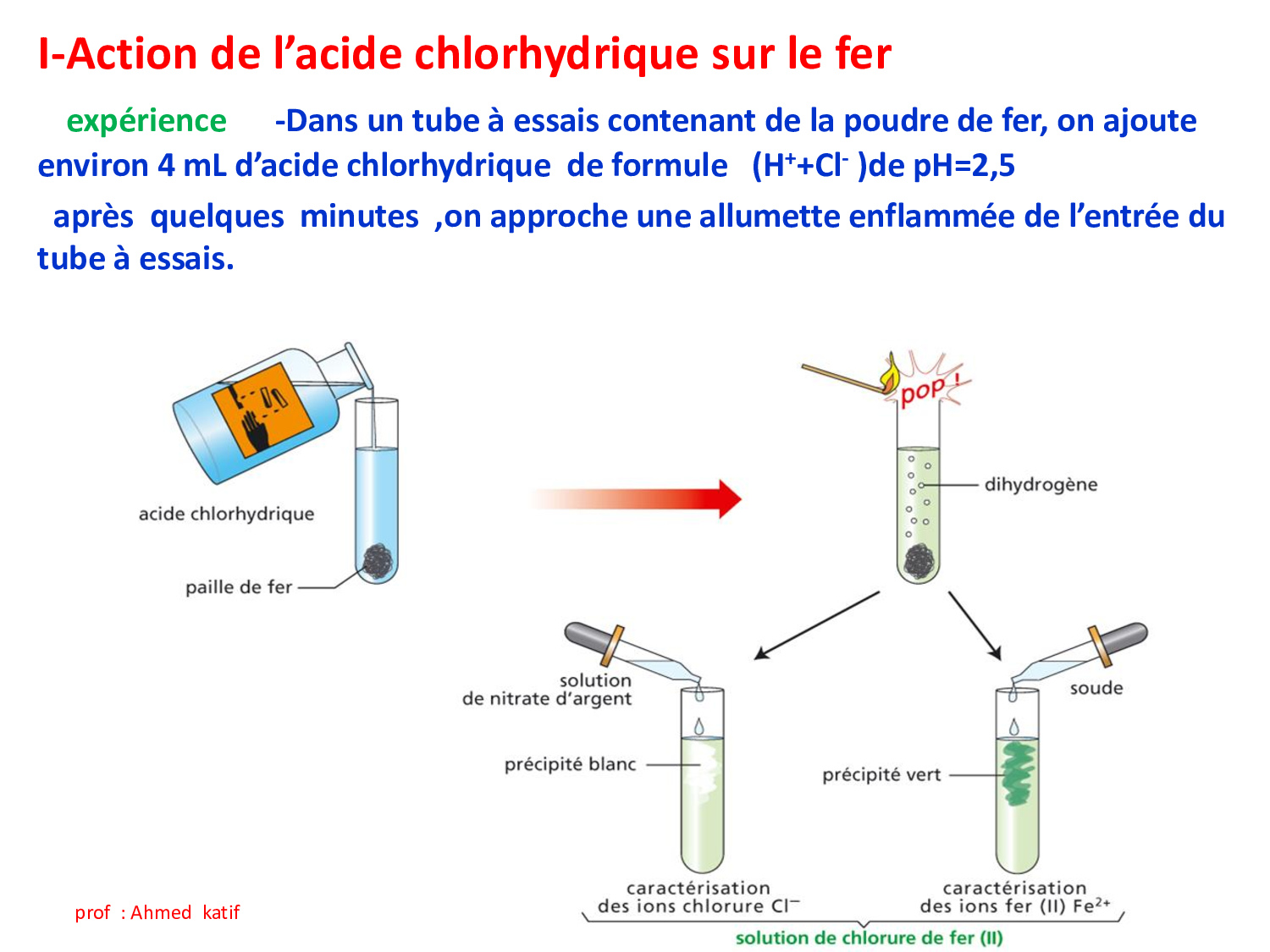
Réactions de quelques métaux avec les solutions acides et basiques Cours 5 AlloSchool

Chimie en solution Les acides et les bases YouTube

Les réactions acidobasiques Résumé de cours 1 AlloSchool

Acides et bases selon Brönsted cours Tle Physiquechimie

Les solutions acides et basiques Cours 1 AlloSchool

1 Les acides et les bases Réactions en
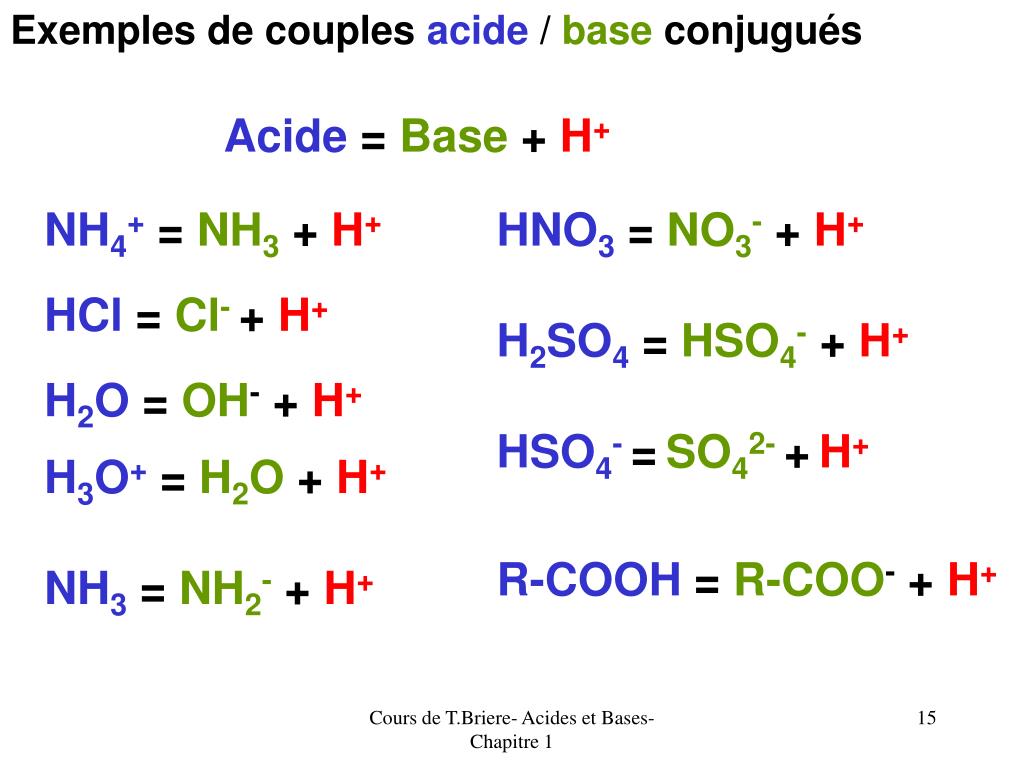
PPT ACIDES ET BASES PowerPoint Presentation, free download ID3849647

TRANSFORMATIONS ACIDOBASIQUE

Equation de réaction acide base CHIMIE TERMINALE YouTube

Équation de réaction acide base ️ Exercice Terminale Chimie YouTube

Les transformations acidebase, couple acide/base YouTube

COURS Réactions acidobasique 1 SMPC YouTube
La réaction acido-basique entre un acide fort et une base forte est toujours une réaction totale et quasi-instantanée. L'acide et la base étant totalement dissociés dans l'eau, la réaction s'écrit : \ce {H3O+}+\ce {OH-}\ce {->}\ce {2H2O} On considère la réaction entre l'acide chlorhydrique et la soude dans l'eau :. Couples acide-base et constantes d'acidité à 25 °C . n°. noms des acides: formules: bases conjuguées: K a: 1: acide iodhydrique: HI: I -± 10 10: 2: acide perchlorique: HClO 4: ClO 4 -± 4.10 8: 3: acide bromhydrique: HBr: Br -± 10 8: 4: acide chlorhydrique: HCl: Cl -± 10 6: 5: acide sulfurique (I) H 2 SO 4: HSO 4 -± 10 4: 6: acide.